സിൽവർ ഓക്സൈഡ്
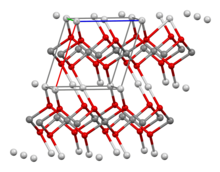
ദൃശ്യരൂപം
 | |
| Names | |
|---|---|
| IUPAC name
silver(I,III) Oxide
| |
| Other names
silver peroxide, argentic oxide, silver suboxide, divasil, tetrasilver tetraoxide
| |
| Identifiers | |
| |
3D model (JSmol)
|
|
| ECHA InfoCard | 100.013.726 |
| EC Number |
|
PubChem CID
|
|
| UNII | |
| InChI | |
| SMILES | |
| Properties | |
| തന്മാത്രാ വാക്യം | |
| Molar mass | 0 g mol−1 |
| Appearance | grey-black powder diamagnetic |
| സാന്ദ്രത | 7.48 g/cm3 |
| ദ്രവണാങ്കം | |
| .0027 g/100 mL | |
| Solubility | soluble in alkalis |
| Hazards | |
| GHS pictograms |   
|
| GHS Signal word | Danger |
| H272, H315, H319, H335 | |
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
| |
വെള്ളിയുടെ ഒരു സംയുക്തമാണ് സിൽവർ(I,III) ഓക്സൈഡ് അല്ലെങ്കിൽ ടെട്രാസിൽവർ ടെട്രാഓക്സൈഡ്. Ag4O4 എന്ന രാസസൂത്രമുള്ള അജൈവ സംയുക്തമാണിത് . സിൽവർ സിങ്ക് ബാറ്ററികളിലെ ഒരു ഘടകമാണ് ടെട്രാസിൽവർ ടെട്രാഓക്സൈഡ്.
ഒരു പെർസൾഫേറ്റ് ലായനിയിൽ ഒരു സിൽവർ ലവണം സാവധാനത്തിൽ ചേർത്തുകൊണ്ട് ഇത് തയ്യാറാക്കാം. (ഉദാ: AgNO3 ഒരു Na2S2O8 ലായനിയിലേക്ക്). [1] ഒരു മിക്സഡ്-വാലൻസ് സംയുക്തമായതിനാൽ ഇത് അസാധാരണമായ ഒരു ഘടന സ്വീകരിക്കുന്നു. [2] വെള്ളത്തിലെ O2 ന്റെ പരിണാമത്തോടെ വിഘടിക്കുന്ന ഇരുണ്ട തവിട്ടുനിറത്തിലുള്ള ഖരമാണ് ഇത്. ഇത് സാന്ദ്രീകൃത നൈട്രിക് ആസിഡിൽ ലയിച്ച് Ag2+ അയോൺ അടങ്ങിയ ബ്രൗൺ ലായനി ഉണ്ടാകുന്നു.[3]
അവലംബം
[തിരുത്തുക]- ↑ Wells A.F. (1984) Structural Inorganic Chemistry 5th edition Oxford Science Publications ISBN 0-19-855370-6
- ↑ David Tudela "Silver(II) Oxide or Silver(I,III) Oxide?" J. Chem. Educ., 2008, volume 85, p 863. doi:10.1021/ed085p863
- ↑ Peter Fischer, Martin Jansen "Electrochemical Syntheses of Binary Silver Oxides" 1995, vol. 30, pp. 50–55. doi:10.1002/9780470132616.ch11
വർഗ്ഗങ്ങൾ:
- Chemical articles with multiple compound IDs
- Multiple chemicals in an infobox that need indexing
- Chemical articles with multiple CAS registry numbers
- Articles without InChI source
- Chemical pages without ChemSpiderID
- Articles without EBI source
- Articles without KEGG source
- ECHA InfoCard ID from Wikidata
- Chembox having GHS data
- സിൽവർ സംയുക്തങ്ങൾ
